O tajemniczych „kroplach życia”, które organizują chaos w naszych komórkach, i o ich mrocznej stronie, która prowadzi do chorób.
Pamiętasz, co mówili w szkole?
Że komórka to taka zupa, w której pływają organelle? Jądro, mitochondria, każde zamknięte w swojej własnej, szczelnej torebce z błony. Porządek musi być. To było proste, logiczne.
A co, jeśli powiem ci, że to tylko połowa prawdy? Co, jeśli w tej zupie, bez żadnych torebek, spontanicznie pojawiają się i znikają miniaturowe, płynne strefy? Takie kropelki życia, które organizują chaos, przyspieszają reakcje, działają jak centra logistyczne.
To nie jest żadne voodoo. To jest liquid-liquid phase separation (LLPS), czyli separacja fazowa ciecz-ciecz. I to jest jeden z najgorętszych tematów w biologii. Zrozumienie tego fenomenu wywraca do góry nogami wszystko, co wiedzieliśmy o tym, jak działa życie. I co ważniejsze, otwiera nowe drzwi do zrozumienia najgorszych chorób ludzkości – Alzheimera, Parkinsona, nowotworów.
Dla ciebie, jako przyszłego doktoranta, to jest szansa na wejście na sam front naukowej rewolucji. Ale jak się za to zabrać? Jak badać coś, co jest płynne, dynamiczne i niewidoczne gołym okiem?
Co to jest to całe LLPS? Myśl jak o oliwie i wodzie.
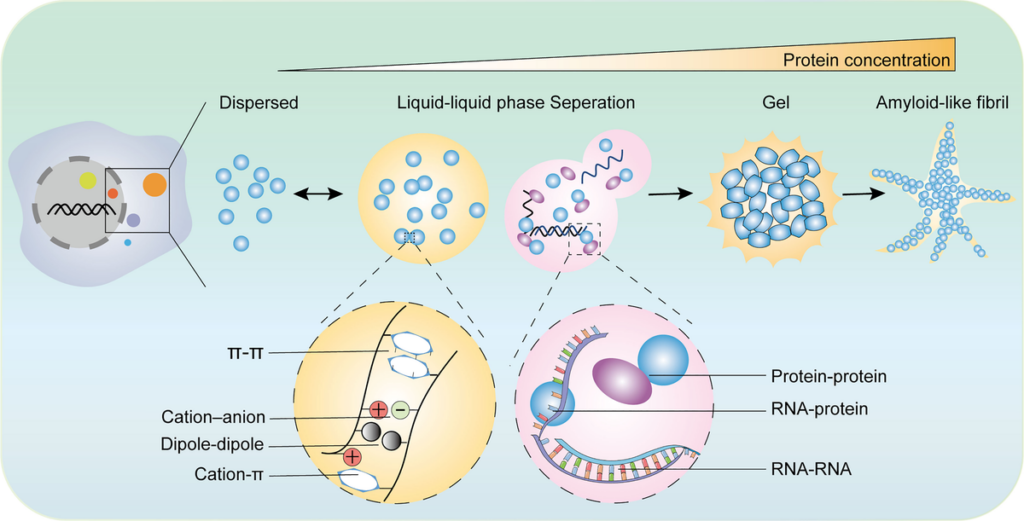
W najprostszych słowach, LLPS to proces, w którym białka i RNA w komórce, zamiast pływać sobie losowo, nagle zbierają się razem i tworzą gęste, płynne krople. Tak jak oliwa w wodzie. Nie ma żadnej błony, żadnej ściany. To czysta fizyka. Słabe oddziaływania między cząsteczkami sprawiają, że wolą one być razem niż osobno.
Te kropelki – zwane kondensatami biomolekularnymi – to super-wydajne mikro-fabryki. Skupiają w jednym miejscu wszystko, co potrzebne do konkretnego zadania, np. naprawy DNA. A kiedy zadanie jest wykonane, rozpuszczają się. Genialne.
Ale jest też mroczna strona tej historii. Czasem te płynne, dynamiczne kropelki zaczynają „twardnieć”. Zamiast się rozpuścić, zamieniają się w stałe, toksyczne grudki. W agregaty, które zabijają komórki. I to jest właśnie to, co widzimy w mózgach pacjentów z chorobami neurodegeneracyjnymi. Płynne życie zamienia się w twardą śmierć.
I właśnie ten związek między zdrowiem a chorobą sprawia, że ten temat jest tak cholernie ważny.
Jak to badać? Przewodnik dla odważnych.
Badanie LLPS to jak bycie detektywem na trzech różnych frontach.
Krok 1: Praca papierkowa (przy komputerze).
Zanim wejdziesz do labu, odpal komputer. Istnieją programy, które potrafią przeanalizować sekwencję twojego ulubionego białka i powiedzieć: „Hej, to białko ma potencjał, żeby tworzyć te kropelki!”. Szukają w nim specyficznych cech – długich, elastycznych ogonów, pewnych aminokwasów. To jest twoja pierwsza poszlaka.
Krok 2: Odtworzenie sceny zbrodni (w probówce).
To jest złoty standard. Bierzesz oczyszczone białko, wkładasz do probówki, zmieniasz warunki (temperaturę, stężenie soli) i patrzysz pod mikroskopem. Czy tworzą się piękne, okrągłe kropelki? Jeśli tak, to jesteś w domu. Ale to nie wszystko. Musisz udowodnić, że są płynne, a nie że to zwykły osad. Jak?
- Test lasera (FRAP): Świecisz laserem w kawałek kropelki, „wypalając” fluorescencję. Jeśli jest płynna, nowe, świecące cząsteczki szybko wpłyną na to miejsce.
- Test fuzji: Patrzysz, czy dwie kropelki, kiedy się dotkną, łączą się w jedną, większą. Jak krople deszczu na szybie.
Krok 3: Sprawdzenie alibi (w żywej komórce).
Super, działa w probówce. Ale czy tak samo jest w żywej komórce? Wprowadzasz do komórki gen kodujący twoje białko ze świecącym znacznikiem (np. GFP). Patrzysz pod mikroskopem, czy tworzy ono w komórce takie same świecące punkciki. I znowu robisz test lasera (FRAP), żeby sprawdzić, czy są dynamiczne.
Krok 4: Most do ciemnej strony (jak płyn zamienia się w truciznę).
Jeśli twoje białko jest związane z jakąś chorobą, to jest najważniejszy krok. Obserwujesz te kropelki przez wiele godzin, dni. Czy zmieniają kształt? Twardnieją? Czy przestają być płynne (sprawdzasz to, powtarzając test FRAP)? Czy zaczynają świecić po dodaniu specjalnego barwnika, który wykrywa toksyczne agregaty? To jest moment, w którym biologia komórki spotyka się z medycyną.
Najczęstsze pułapki (i jak w nie nie wpaść)
- To nie osad, to kropla! Jeśli widzisz pod mikroskopem nieregularne, brzydkie grudki, to prawdopodobnie nie jest LLPS. Pamiętaj: test FRAP i fuzja to twoi najlepsi przyjaciele.
- Nie zmuszaj komórki do kłamania. Jak wpakujesz do komórki sto razy więcej białka, niż ma normalnie, to prawie wszystko zacznie się zlepiać. Zawsze staraj się potwierdzić swoje wyniki na naturalnym poziomie białka.
- Jeden dowód to żaden dowód. W tej dziedzinie musisz być jak prokurator. Potrzebujesz wielu niezależnych dowodów, żeby zbudować solidną sprawę.
Twoja szansa na przełom.
Badanie LLPS to nie jest jakaś niszowa zabawa. To jest fundamentalna zmiana w myśleniu o życiu. Doktorat w tej dziedzinie to szansa na zrobienie czegoś, co jest na absolutnej granicy poznania. Ale to też wyzwanie. Wymaga łączenia wiedzy z biologii, fizyki, chemii. Wymaga opanowania masy trudnych technik.
Jeśli czujesz ten dreszcz ekscytacji, ale jednocześnie przeraża cię ogrom tego zadania, nie musisz przez to przechodzić sam.
Publikacje i badania wykonane przez nas
A to kilka przykładów z naszego podwórka, które pokazują, jak w praktyce badamy te złożone, dynamiczne procesy:
- Charakterystyka biofizyczna kondensatów formowanych przez białko FUS i jego mutanty związane z ALS, w celu zrozumienia mechanizmu przejścia od płynnych kropli do stałych agregatów.
- Opracowanie nowego, fluorescencyjnego sensora do badania zmian w lepkości i dynamice wewnątrz organelli bezbłonowych w żywych komórkach.
- Analiza roli długich, niekodujących RNA jako rusztowań (scaffolds) dla kondensatów zaangażowanych w odpowiedź na stres komórkowy.
- Badanie wpływu modyfikacji potranslacyjnych (np. fosforylacji) na zdolność białka tau do separacji fazowej i jego związku z patogenezą choroby Alzheimera.
- Screening biblioteki małych cząsteczek pod kątem związków, które modulują (rozpuszczają lub stabilizują) kondensaty formowane przez białka związane z chorobami neurodegeneracyjnymi, jako potencjalna strategia terapeutyczna.
#biologiakomórki #doktorat #LLPS #agregacjabiałek #nauka