Sztuczna inteligencja w medycynie to obietnica rewolucji, zwłaszcza w radiologii. Wizja algorytmu, który z nadludzką precyzją wykrywa najwcześniejsze stadia raka na zdjęciach mammograficznych, rozpala wyobraźnię pacjentów i lekarzy. Dostępne na rynku systemy AI rzeczywiście wykazują imponującą skuteczność, często dorównując lub przewyższając ludzkich ekspertów w ogólnej detekcji zmian. Jednak w medycynie, a szczególnie w onkologii, średnie i ogólniki nie wystarczą. Liczy się każdy, pojedynczy przypadek.
Nowe, rygorystyczne badanie przeprowadzone przez koreański zespół naukowców, rzuca na tę obietnicę snop otrzeźwiającego światła. Analiza pokazuje, że nawet najlepsze algorytmy mają swoje „martwe pola”. Pomijają one znaczący odsetek inwazyjnych nowotworów piersi – tych, w których opóźnienie diagnozy ma bezpośredni wpływ na szanse przeżycia pacjentki. Zrozumienie, czego AI nie widzi, jest dziś równie ważne, jak zachwyt nad tym, co potrafi wykryć.
Sztuczna inteligencja pod lupą: niewidoczne oblicze raka piersi
Celem badania, opublikowanego w prestiżowym czasopiśmie „Radiology”, była szczegółowa analiza błędów popełnianych przez komercyjnie dostępny program AI w diagnostyce mammograficznej. Zespół naukowców z Korea University College of Medicine przeanalizował 1097 przypadków raka piersi zdiagnozowanych w latach 2014-2020, aby sprawdzić, ile z nich system AI by przeoczył.
Kluczowym celem była ocena skuteczności w wykrywaniu raka inwazyjnego (stadia 1-4), który nacieka otaczające tkanki, w odróżnieniu od raka nieinwazyjnego, ograniczonego do przewodów mlekowych (stadium 0). Wyniki okazały się alarmujące.
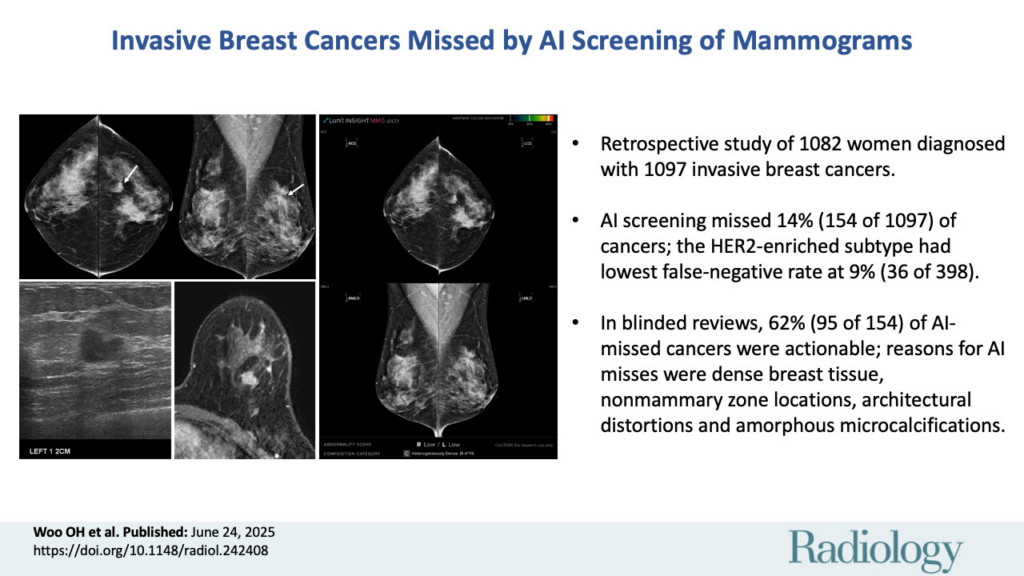
AI przeoczyło łącznie 14% wszystkich inwazyjnych nowotworów piersi.
Analiza w podziale na podtypy biologiczne nowotworu pokazała jeszcze większe zróżnicowanie w skuteczności algorytmu.
| Podtyp biologiczny raka piersi | Odsetek przypadków przeoczonych przez AI |
| Typ luminalny | 17,2% |
| Trójnegatywny | 14,5% |
| HER2-pozytywny | 9,0% |
Profil „niewidzialnego” nowotworu: czego nie dostrzega algorytm?
Najważniejszym wkładem badania jest precyzyjne scharakteryzowanie guzów, które najczęściej umykają uwadze sztucznej inteligencji. Okazuje się, że istnieje wyraźny profil nowotworów, przy których algorytm jest mniej skuteczny.
Cechy inwazyjnych raków piersi najczęściej omijanych przez AI:
- Występowały u młodszych kobiet.
- Były to małe guzy (poniżej 2 cm).
- Charakteryzowały się niższym stopniem złośliwości histologicznej.
- Rzadziej dawały przerzuty do węzłów chłonnych.
- Wykazywały niską ekspresję antygenu Ki-67 (wskaźnik proliferacji komórek).
- Były zlokalizowane poza obszarami tkanki gruczołowej.
Co jednak najbardziej uderzające, analiza wykazała, że ponad 60% (dokładnie 61,7%) tych przeoczonych przez AI nowotworów zostało uznanych za wykrywalne przez doświadczonych radiologów.
Dlaczego AI popełnia błędy? Przyczyny techniczne
Badanie zidentyfikowało również najczęstsze przyczyny radiologiczne, dla których AI zawodziło. Były to:
- Gęsta tkanka piersi, która na obrazie mammograficznym może maskować zmiany nowotworowe.
- Lokalizacja guza poza tkanką gruczołową.
- Obecność zaburzeń architektoniki tkanki zamiast wyraźnego guza.
- Występowanie mikrozwapnień jako jedynego objawu.
Synergia, nie zastępstwo: jaka jest rola AI w radiologii?
Wyniki tego badania nie oznaczają, że sztuczna inteligencja jest bezużyteczna w diagnostyce raka piersi. Wręcz przeciwnie, potwierdzają jej ogromną siłę, ale jednocześnie brutalnie obnażają jej ograniczenia. Główny wniosek, jak podsumowuje profesor Sungeun Song, jest jednoznaczny:
„Chociaż AI wykazuje wysoką skuteczność w wykrywaniu raka piersi, nasze odkrycia podkreślają potrzebę ciągłego nadzoru i komplementarnej pracy ze strony radiologów”.
AI nie jest autonomicznym diagnostą, ale niezwykle potężną „drugą parą oczu” dla lekarza. To narzędzie wspomagające, które może pomóc wychwycić zmiany, ale nie może zastąpić ostatecznej oceny i kontekstowego rozumienia, które wnosi ludzki ekspert. Zrozumienie, jakie cechy nowotworów są „trudne” dla AI, jest kluczowe zarówno dla ulepszania przyszłych algorytmów, jak i dla bezpiecznego wdrażania obecnych narzędzi w codziennej praktyce klinicznej.
FAQ – Najczęściej zadawane pytania
- Czy to badanie oznacza, że nie powinnam ufać diagnozie AI?
Nie. Oznacza to, że nie należy ufać wyłącznie diagnozie AI. W praktyce klinicznej systemy AI działają jako wsparcie dla radiologa. Lekarz analizuje obraz, a następnie sprawdza sugestie AI. To połączenie ludzkiej wiedzy i mocy obliczeniowej maszyny daje najlepsze rezultaty. - Czym jest gęsta tkanka piersi i dlaczego jest problemem w mammografii?
Piersi składają się z tkanki tłuszczowej, gruczołowej i włóknistej. „Gęsta tkanka” to taka, w której dominuje tkanka gruczołowa i włóknista. Na obrazie mammograficznym obie te tkanki, jak i nowotwory, są widoczne jako białe obszary. W gęstej piersi guz może być „ukryty” w białym tle, co utrudnia jego wykrycie zarówno przez człowieka, jak i przez AI. - Dlaczego AI częściej omijało mniejsze guzy u młodszych kobiet?
Młodsze kobiety częściej mają gęstą strukturę piersi, co, jak wyjaśniono wyżej, utrudnia detekcję. Mniejsze guzy z definicji dają subtelniejszy obraz na mammogramie, co czyni je trudniejszymi do odróżnienia od tła. To pokazuje, że AI, podobnie jak ludzie, ma największe problemy z najtrudniejszymi diagnostycznie przypadkami. - Co oznaczają podtypy biologiczne raka piersi (luminalny, trójnegatywny, HER2-dodatni)?
Są to klasyfikacje oparte na obecności lub braku określonych receptorów na powierzchni komórek nowotworowych (estrogenowych, progesteronowych i receptora HER2). Ta klasyfikacja jest kluczowa dla doboru odpowiedniego leczenia (np. hormonoterapii, terapii celowanej). Badanie pokazało, że skuteczność AI może się różnić w zależności od tych fundamentalnych cech biologicznych guza. - Jaka jest przyszłość AI w mammografii w świetle tego badania?
Przyszłość leży w synergii i specjalizacji. Zamiast dążyć do stworzenia jednego, uniwersalnego algorytmu, rozwój pójdzie w kierunku modeli wyspecjalizowanych w trudnych przypadkach, np. w analizie gęstej tkanki. Kluczowe będzie również tworzenie systemów, które nie tylko wskazują zmianę, ale także komunikują lekarzowi poziom swojej niepewności, sygnalizując, kiedy potrzebny jest szczególnie wnikliwy nadzór człowieka.